Impact du dépistage de la pré-éclampsie au premier trimestre de la grossesse
Une large étude française multicentrique évaluant l’intérêt du dépistage de la pré-éclampsie pour améliorer la santé des mères et des enfants
Pourquoi l’étude RANSPre ?
La pré-éclampsie est une complication survenant en deuxième moitié de grossesse et caractérisée par la présence d’une hypertension artérielle associée à une protéinurie (présence d’un taux anormalement élevé de protéines dans les urines). Elle touche 2% des femmes enceintes, soit 15 000 patientes chaque année en France. C’est une pathologie potentiellement grave pour la mère et son enfant.
La pré-éclampsie est liée à un dysfonctionnement du placenta. Il n’y a actuellement pas de traitement de la pré-éclampsie, une fois celle-ci présente, et seul l’accouchement – permettant le retrait du placenta – est associé à une régression des anomalies cliniques et biologiques. Cependant, l’accouchement doit parfois être réalisé précocement exposant l’enfant aux complications de la prématurité.
Un traitement préventif de la pré-éclampsie, c’est-à-dire un traitement permettant d’éviter sa survenue, existe. Il s’agit de l’aspirine prescrite à faible dose, entre 100 et 160 mg par jour. Ce traitement est d’autant plus efficace qu’il est prescrit tôt dans la grossesse. En France ce traitement est recommandé pour les femmes enceintes ayant eu une pré-éclampsie lors d’une grossesse précédente.
D’autres facteurs de risque de pré-éclampsie sont connus mais nous ne savons actuellement pas comment ils peuvent être intégrés dans l’indication d’un traitement préventif par aspirine. Plusieurs pays anglo-saxons recommandent la prescription d’aspirine chez les femmes ayant ces facteurs de risque ce qui augmente de façon importante le nombre de femmes enceintes qui reçoivent ce traitement (jusqu’à 30%).
Un test de dépistage (« Fetal Medicine Foundation triple test ») permettant d’estimer dès le premier trimestre de la grossesse le risque de survenue d’une pré-éclampsie existe. Ce test intègre des paramètres maternels cliniques (âge, nombre de grossesses antérieures, antécédents maternels, origine géographique, tabagisme, modalités de conception, poids, pression artérielle), des paramètres échographiques (résistances des flux sanguins des artères utérines) et des paramètres biologiques (dosage sanguin maternel du Placental Growth Factor).
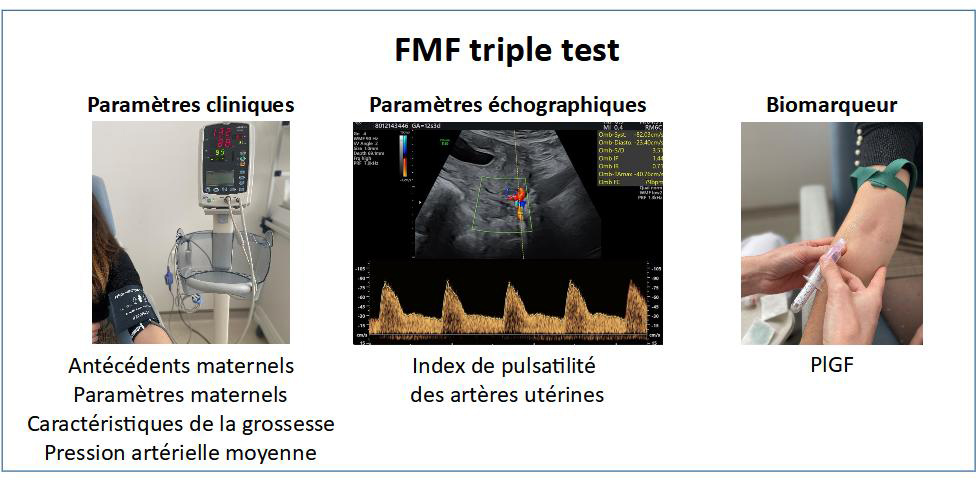
Ce dépistage combiné permet d’identifier des femmes à risque de développer une pré-éclampsie en plus de celles qui ont un antécédent de pré-éclampsie et permettrait de mieux cibler les indications d’un traitement par aspirine pendant la grossesse. Ce dépistage n’est actuellement pas intégré aux soins courants en routine car les bénéfices et les effets secondaires potentiels pour la santé des femmes et des nouveau-nés ne sont pas connus. En effet, nous ne disposons pas à ce jour d’étude randomisée (c’est-à-dire avec tirage au sort) évaluant cette stratégie de dépistage et comparant des femmes bénéficiant de ce dépistage à des femmes bénéficiant d’une prise en charge habituelle.
Et si un dépistage précoce de la pré-éclampsie permettait de réduire l’incidence de cette pathologie et ses complications ?
Quels sont les objectifs de l’étude RANSPre ?
Cette étude a pour objectif principal d’évaluer l’intérêt de réaliser un dépistage systématique de la pré-éclampsie au 1er trimestre de la grossesse, sur la santé des mères et des enfants.
Les objectifs secondaires sont d’évaluer l’impact de ce dépistage sur la satisfaction des femmes enceintes et sur les coûts de prise en charge.
Cette étude permettra également d’évaluer les performances prédictives du test combiné en population française ainsi que la faisabilité de sa mise en œuvre.
Pour en savoir plus : https://clinicaltrials.gov/ct2/show/NCT05521776/ (en anglais)
Qui peut participer à l’étude RANSPre ?
Toute femme enceinte au 1er trimestre de la grossesse est éligible si :
- sa grossesse est monofoetale (un seul enfant) et évolutive ( entre 11 et 14 semaines )
- elle est majeure
- elle possède une couverture assurance maladie ( y compris l’AME )
Un antécédent de pré-éclampsie lors d’une précédente grossesse et une contre-indication à l’aspirine sont des critères de non inclusion.
En quoi consiste l’étude RANSPre ?
L’étude RANSPre est proposée par l’équipe soignante de la maternité de suivi, lors de la consultation habituelle pour l’échographie du premier trimestre.
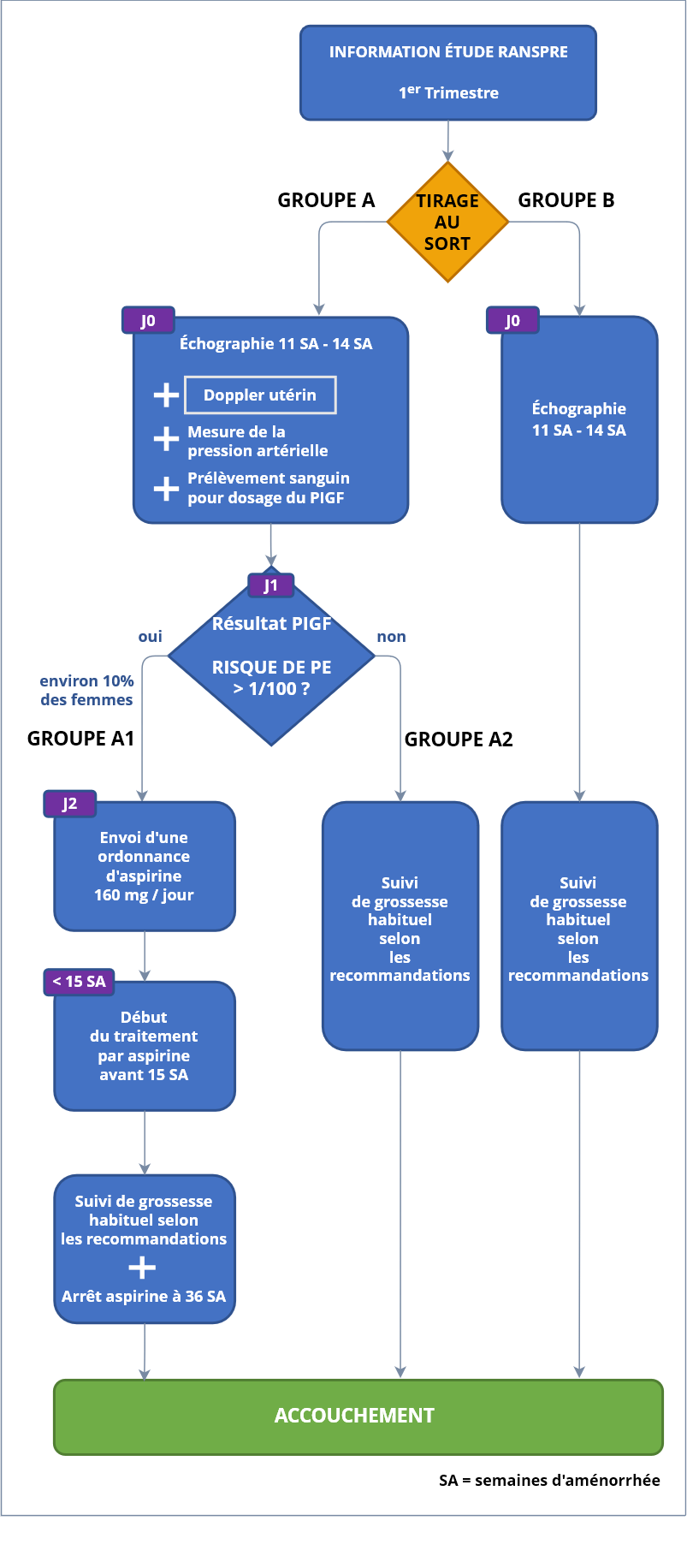
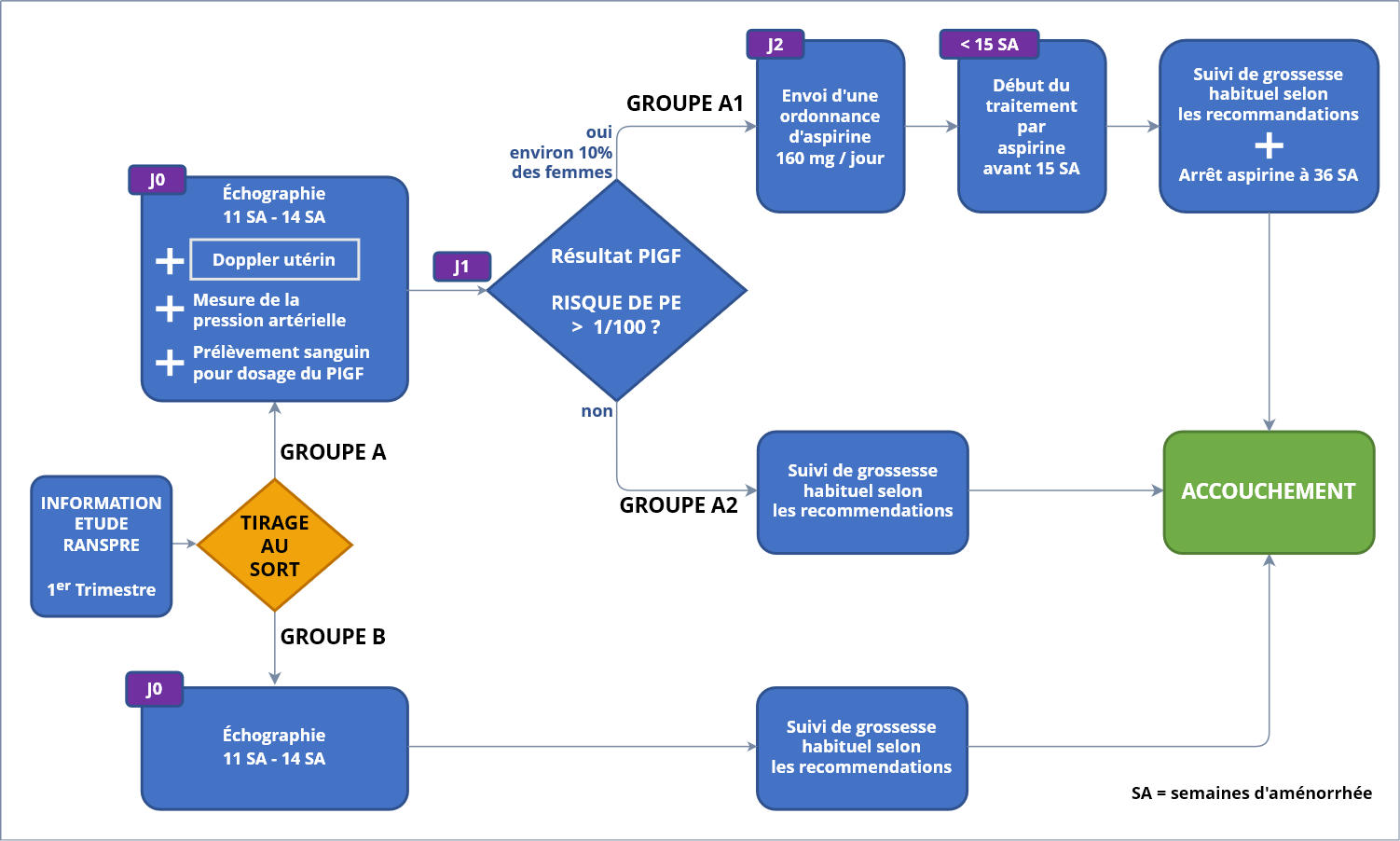
Pour toute patiente acceptant de participer à cette étude, un tirage au sort permet de déterminer le groupe dans lequel elle sera prise en charge :
- Groupe A avec dépistage de la pré-éclampsie
- réalisation (le jour de la consultation pour l’échographie ou dans les 3 jours) d’un Doppler des artères utérines (complément de l’échographie, cliquez sur l’image pour lire la vidéo) et d’une prise de sang

- calcul de risque (selon l’algorithme) :
- Groupe A1 : Si le test de dépistage est « positif » (c’est-à-dire si le risque estimé de prééclampsie est >1/100), un traitement par aspirine sera débuté et pris jusqu’à 36 semaines, et la grossesse sera par ailleurs suivie selon les recommandations habituelles
- Groupe A2 : Si le test de dépistage est « négatif » (c’est-à-dire si le risque estimé de prééclampsie est <=1/100) la grossesse sera suivie selon les recommandations habituelles
- réalisation (le jour de la consultation pour l’échographie ou dans les 3 jours) d’un Doppler des artères utérines (complément de l’échographie, cliquez sur l’image pour lire la vidéo) et d’une prise de sang
- Groupe B sans dépistage de la pré-éclampsie avec suivi de grossesse habituel
RANSPre est une étude française financée par le Ministère des Solidarités et de la Santé (programme PHRC). Il s’agit d’une étude académique sans participation financière des industriels.
Au total l’objectif est d’inclure 14 500 patientes sur 2 ans, à compter du 1er Novembre 2022.
Maternités participantes
Les 21 maternités participant à l’étude RANSPre font partie du Groupe de Recherche en Gynécologie et Obstétrique (GROG). Elles sont réparties dans 17 villes.
Comment participer à l’étude RANSPre ?
Si vous souhaitez participer à RANSPre, il est nécessaire que votre maternité fasse partie de l’étude. Vous pouvez en discuter avec l’équipe qui vous suit et/ou nous contacter par mail via l’adresse : etude.ranspre.cch@aphp.fr
Voici la fiche d’information patiente de l’étude RANSPre : FICHE D’INFORMATION
L’équipe RANSPre

Pr Vassilis TSATSARIS
Investigateur Coordonnateur
Maternité Port Royal (Paris)

Dr Catherine DENEUX
Directrice scientifique
INSERM Équipe EPOPé (Paris)

Pr Jean GUIBOURDENCHE
Biologiste
Hôpital Cochin (Paris)

Natasha CARETTI
Sage-femme coordinatrice
Maternité Port Royal (Paris)
Promoteur : AP-HP
Les partenaires de l’étude RANSPre








Pour en savoir plus sur la pré-éclampsie et l’étude RANSPre
L’association d’usagers Grossesse Santé contre la Pré-Eclampsie : https://www.grossesse-sante.org
Un MOOC sur la pré-éclampsie : https://www.fhu-prema.org/enseignement/mooc-et-e-learning/mooc-pre-eclampsie/
Dossier pré-éclampsie de l’INSERM : https://www.inserm.fr/dossier/pre-eclampsie/
Références bibliographiques
1. Chappell L, Cluver CA, Kingdom J, Tong S. Pre-eclampsia. Lancet. 2021 July 24;398:341-354.
2. Lecarpentier E, Fournier T, Guibourdenche J, Tsatsaris V. Pathophysiology of preeclampsia. Presse Med. 2016 Jul-Aug;45(7-8 Pt 1):631-7.
3. Atallah A, Lecarpentier E, Goffinet F, Doret-Dion M, Gaucherand P, Tsatsaris V. Aspirin for Prevention of Preeclampsia. Drugs. 2017 Nov;77(17):1819-1831.
4. Rolnik DL, Nicolaides KH, Poon LC. Prevention of preeclampsia with aspirin. Am J Obstet Gynecol. 2020 Aug 21:S0002-9378(20)30873-5.
5. Askie LM, Duley L, Henderson-Smart DJ, Stewart LA; PARIS Collaborative Group. Antiplatelet agents for prevention of pre-eclampsia: a meta-analysis of individual patient data. Lancet. 2007 May 26;369(9575):1791-1798.
6. Roberge S, Bujold E, Nicolaides KH. Aspirin for the prevention of preterm and term preeclampsia: systematic review and metaanalysis. Am J Obstet Gynecol. 2018 Mar;218(3):287-293.e1.
7. Société française d’anesthésie et de réanimation (Sfar); Collège national des gynécologues et obstétriciens français (CNGOF); Société française de médecine périnatale (SFMP); Société française de néonatalogie (SFNN). Multidisciplinary management of severe pre-eclampsia (PE). Experts’ guidelines 2008. Société française d’anesthésie et de réanimation. Collège national des gynécologues et obstétriciens français. Société française de médecine périnatale. Société française de néonatalogie. Ann Fr Anesth Reanim. 2009 Mar;28(3):275-81.
8. Mounier-Vehier C, Amar J, Boivin JM, Denolle T, Fauvel JP, Plu-Bureau G, Tsatsaris V, Blacher J. Hypertension and pregnancy. Expert consensus statement from the French Society of Hypertension, an affiliate of the French Society of Cardiology. Presse Med. 2016 Jul-Aug;45(7-8 Pt 1):682-99.
9. Lecarpentier É, Vieillefosse S, Haddad B, Fournier T, Leguy MC, Guibourdenche J, Tsatsaris V. Placental growth factor (PlGF) and sFlt-1 during pregnancy: physiology, assay and interest in preeclampsia. Ann Biol Clin (Paris). 2016 Jun1;74(3):259-67.
10. Poon LC, Kametas NA, Maiz N, Akolekar R, Nicolaides KH. First-trimester prediction of hypertensive disorders in pregnancy. Hypertension. 2009 May;53(5):812-8.
11. Wright D, Tan MY, O’Gorman N, Poon LC, Syngelaki A, Wright A, Nicolaides KH. Predictive performance of the competing risk model in screening for preeclampsia. Am J Obstet Gynecol. 2019 Feb;220(2):199.e1-199.e13.